时间:2019-10-17 15:26
来源: 汪亮
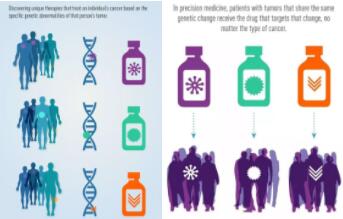
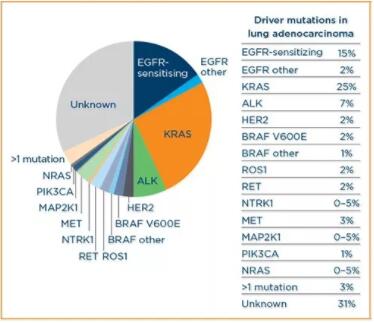
“基因数据对于新药研发而言,正如用户画像之于互联网”。 图1:《女狙击手》剧照(来源/新浪) “能帮我介绍一个基因公司吗,我家人得了乳腺癌,医生推荐用靶向药/免疫治疗前做个基因检测……” 每隔一段时间,笔者经常听到身边的人收到这样的问题。 靶向药以及免疫治疗和基因检测有什么关系?这就是本文讨论的伴随诊断。 2018年12月,帕捷特(帕妥珠单抗)在国内上市,成为第二个靶向HER2阳性乳腺癌的新药。虽然距离第一个上市的同类药物赫赛汀(曲妥珠单抗)已过去16年。但得益于国内政策,帕捷特在我国的价格不到美国的1/4,在内地的价格也比香港低20%。 同时,患者不得不面临另外一组数据,“降价”后的帕捷特在国内全疗程(约18个周期,19支)的费用超过约35万元。通过降低关税和纳入医保等政策,国家在推动降低重疾新药的费用。另外的问题出来了,花去30多万元,如何快速确认药物是否有效,肿瘤出现耐药了吗? 这时候基于基因检测等技术的伴随诊断就发挥作用了。 一、好拍档:新药狙击手和基因观察员 从2017年起,创新药的研发和应用在我国得到大力推动,已成为基本国策。比如,IND(新药临床试验申请)审批执行默认许可(60个工作日),审批时间从10-16个月缩减到最长3个月[1]。 同时,2019年我国批准的肿瘤新药仅为FDA的1/3;纵观全球,临床试验的平均成功率仅为10%[2]。面对传统“10年10亿”的新药研发长周期大投入,除了降低抗癌药等关税,引进外资外,如何实现后发突围,精准狙击? 需要一个拍档:基因捕手。 NMPA药品审评中心化药临床一部部长杨志敏在CSCO 2019年会表示 ,加速创新药临床开发的重中之重是基础研究,其次是检测技术、靶向治疗和免疫治疗等治疗技术创新以及模式创新。在模式创新方面,除了II期和III期无缝临床试验和平台化外,生物标志物富集设计以及伞式/篮式设计是重要的方面。 杨部长提到的生物标志物中,基因是目前从分子层面数字化、高通量读写的最常用的生物标志物之一。而伞式和篮式设计分别对应“异病同治”和“同病异治”(注:伞式设计,即根据不同的靶基因对同一疾病分子分型而采用不同的药物;篮式设计,即将带有相同靶基因的不同疾病放进一个篮子里进行研究,如图2)。 图2:(左)伞式设计和“同病异治”,(右)篮式设计和“异病同治”(来源/NCI,点击图片方法更清晰) 举例来说。“伞式设计”方面,对于众多药企最为关注的癌症之一肺癌,可以通过EGFR、KRAS、等不同驱动基因/突变位点来细分为十余种亚型(如图3),从而对应诞生了针对不同亚型的肺癌靶向药,仅仅EGFR靶向基因即催生了吉非替尼、阿法替尼、奥希替尼等一、二、三代抑制剂。 在“篮式设计”方面,由于ALK基因突变是非小细胞肺癌、淋巴瘤、肾癌、神经母细胞瘤等癌症的驱动基因,从2011-2019年,辉瑞主导的克唑替尼临床试验(NCT01121588)即囊括了上述各种ALK基因靶向的恶性肿瘤临床试验。 图2:肺癌(腺癌)的分子分型(来源/LUNGevity) 除了在基础研究和模式设计层面,具体应用层面,创新药研发和推广中,基因也扮演者重要角色。特别是伴随诊断(Companion Diagnosistic,简称CDx)和DNA编码化合物库(DNA Encoded Compound Library,简称DEL)。 本文先讨论基因伴随诊断和新药研发。
二、创新药研发和伴随诊断的产业势能互补
随着我国医药市场的庞大需求和不断开放,近年跨国药企在我国的步伐不断加快。除了新药生产外包等合作,阿斯利康等药企将橄榄枝抛向头部和中等规模基因企业。
除了和无锡市政府合作打造无锡国际生命科学创新园、和药明康德合作新药生产以及和国投创新合资新药公司外,在2015年4月,阿里斯康组织了一场“阿斯利康肿瘤伴随诊断战略合作伙伴意向沟通会”,受邀对象包括BGI、Illumina(中国)、Thermo Fisher(中国)等头部和中等规模基因企业。 主要对象是三代TKI、治疗BRCA基因突变药物Olaparib和Lynparza等药的伴随诊断。直到2019年,包括和瑞基因、吉因加、鹍远基因、泛生子等肿瘤基因公司陆续披露和阿斯利康的战略合作。同时在2018年8月至12月,阿斯利康、默沙东和Thermo Fisher、Illumina(以上四家均为中国分公司)开展“NGS BRCA校准计划”,吸引了六十余家企业及实验室参与探讨BRCA基因检测需求和规范。
在接受基因慧(微信公众号:GeneClub-1)采访时,吉因加的李清林总监表示,吉因加和阿里斯康合作点主要是基于吉因加的国产测序平台和配套试剂盒,结合阿斯利康的渠道下沉,在三四线城市扩大患者教育和精准用药的覆盖范围。同样和阿里斯康合作的泛生子基因告诉基因慧,目前与阿斯利康的合作囊括了科研大数据,临床及上市后推广,以及一些特定方向的慈善项目及商业化合作尝试等。
阿斯利康兴师动众的肿瘤伴随诊断的意义是什么?
首先我们引用肿瘤基因公司Myriad副总裁Johnathan Lancaste公开的一段话:
伴随诊断工具让我们能够了解癌细胞表型背后的遗传改变。更重要的是,可以使我们能够根据患者自身肿瘤的生物学特性,使患者接受个性化治疗。这是患者感兴趣的事情,因为可以增强治疗信心。
根据美国FDA的定义,伴随诊断的作用体现在:在前期,可以确定哪些患者最有可能受益于特定的治疗产品(包括副作用等);在中后期,监控能够提供患者针对特定治疗药物的治疗反应以便调整治疗。
在实际应用场景中,包括临床指导用药以及临床试验入组两方面。基因慧获悉,目前超过90%是集中在前者,后者主要集中在一线城市有临床试验的PI实验组里。
1998年乳腺癌靶向药赫赛汀(Herceptin)获批,其伴随诊断生物标志物为HER2基因,约20%乳腺癌患者的HER2基因过表达,使用赫赛汀后10年生存期从75%增大至84%。由此开启了靶向药及伴随诊断快速发展时代,截至2019年8月,经过FDA认证或批准的伴随诊断产品已有37种[6]。目前FDA一般是对新药和其伴随诊断产品同时批准上市。
自2014年来,FDA陆续出台伴随诊断相关的规范文件(如表1)。
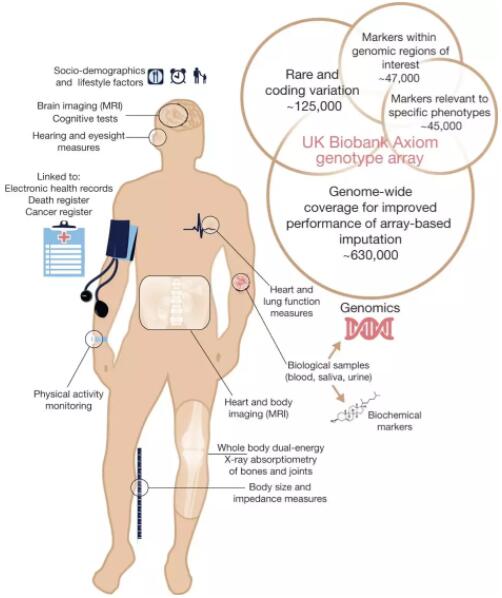
表1:FDA陆续出台伴随诊断相关的规范文件(来源/FDA&基因慧编译) 四、NGS技术作为伴随诊断的趋势 根据Markets&Markets的预测,到2024年,全球伴随诊断市场预计将从2019年的35亿美元增长到73亿美元,复合年增长率为15.7%。基因慧认为这个数字过于保守,忽略了药物研发中成本降低的收益,此是后话。 泛生子基因告诉基因慧,无论是传统的免疫组化,RT-PCR试剂盒,还是近年来新兴的二代测序或数字PCR平台,都能够为病人提供用药前的靶向检测和指导。其中,NGS方法基于其高通量的特性和价格的不断降低,在同等周期和样品量的前提下,可以高效检测多种不同的基因靶点。基因慧认为,随着高通量测序(NGS)技术的普惠,未来的伴随诊断将从目前的小Panel,快速拓展到大Panel以及全基因组,在全生命周期管理上提前关口到新生儿阶段。 在产品商业化(也是技术普惠化)过程中,美国的Foundation Medicine(FMI)、MSK走在前列,国内的艾德生物、燃石医学、世和基因、诺禾致源、华大基因等也取得NMPA的资质。 首个基于高通量测序(NGS)的伴随诊断试剂盒要追溯到2016年12月19日,FMI公司的FoundationFocus CDxBRCA产品获得FDA的批准,主要是检测卵巢癌患者的BRCA基因来判断新药Rubraca是否可能有效。根据Clovis和FMI两家公司的年报,2019年Q2的Rubraca 的净销售额是 3300万美金,同比增长39%。FMI在被Roche收购前的最后一次财报(2018年Q1)显示,临床检测服务达21,861人次,同比增长57%,FoundationFocus CDx BRCA 的销量为48人次,有很大增长空间。 一年后的2017年11月,首个多癌种多基因检测平台获FDA批准:MSK-IMPACT(详情)。实现了从药物疗效相关基因的特异变异位点到整个panel(多基因组合)的跨越,也开创了医学和商业实验室开发的基因检测产品的授权先例。紧接着,FMI的FoundationOne CDx获FDA批准(详情),覆盖324个基因,得到FDA和CMS(医疗保险和医疗补助服务中心)平行审查计划,六个月快速获批。目前在三大洲的20多个国家上市。 癌症诊断公司NeoGenomics(Nasdq:NEO) 今年第二季度营收同比增长50%,截止2019年6月30日的收入达到1.017亿美元,CEO Douglas VanOort谈到,伴随诊断领域期望稳定增长,目前有30个项目正在进行中,预计2020年在中国投入建设实验室。癌症基因检测公司Guardant Health (NASDAQ:GH) 也因针对生物制药客户的伴随诊断开发,Q2营收同比翻了6倍,达到4210万美元。 我国肿瘤基因伴随诊断试剂盒,在ctDNA方面,以2018年1月的艾德生物的Super-ARMS® EGFR开先河,紧接着2018-2019年,在NGS领域陆续审批了包括燃石医学、诺禾致源、世和基因、艾德生物和华大基因五家公司的NGS伴随诊断试剂盒,在其他四家均聚焦非小细胞肺癌同时,艾德生物率先实现跨癌种(结直肠癌)的NGS伴随诊断。 表2:近年各国获批的伴随诊断试剂盒不完全统计(来源/基因慧,点击图片放大更清晰) 四、展望未来 展望未来,基于基因测序、免疫组化等技术的伴随诊断的市场规模持续扩大,同时反哺推动创新药研发,形成正向回路。主要原因和推动力包括以下几点: 图4:英国生物银行(UK Biobank)研究的生物数据(来源/Nature) 1. 基础研究:广义的基因型和表型的持续发现和转化 基因型和表型的研究逐渐趋向大样本队列,形成生物样本库(生物银行)。 2005年起,由英国卫生部联合Wellcome Trust等多家机构启动的英国生物银行(UK Biobank),截止2010年共招募和获得近50万人的生物样本数据(图4)。自开放数据访问以来,超过8000个获批的注册项目,在同行评议期刊上发表了超过500篇文章。例如在一项8,248位个体样本研究中,科学家确定了3000多种大脑功能和结构成像相关表型,并进行了全基因组关联研究,确定部分与神经退行性疾病相关的基因[10]。UK Biobank今年获得安进、阿斯利康、葛兰素史克以及强生四家药企总计投入的1亿英镑。 在我国,自2015年启动的“中国聋病基因组计划”、2016年启动的覆盖超过60万人“精准医学研究”重大专项、2018年启动的“中国十万人基因组计划”等人群队列研究,将持续发现和广义的基因型和表型的关联(包括微生物组、蛋白组等)。在2020-2030年期间,这些建立在中国多样化人群基础上的生物样本,将为药物基因靶点发现、伴随诊断及新药研发提供丰富的素材。 2. 创新药政策推动:外企药及外资开放和审批政策 除了降低抗癌药关税外,在 2017 年新版目录以及后续的谈判目录中,我们可以看到吉非替尼,埃克替尼等17种抗癌药纳入国家医保。基于伴随诊断的精准用药(用药指导)在提高患者精准治疗效率同时,一定程度上通过合理用药来降低医保开支。 此外,2019年10月,作为由美国惠普公司战略重组分立而成的跨国公司安捷伦(NYSE: A) 获得我国首个批准的PD-L1伴随诊断试剂盒,在患者服用默沙东的非小细胞肺癌药物KEYTRUDA时进行用药指导。可以看出我国在创新药领域的开放决心。 国产药企也在加快步伐。国产PD-1/PD-L1上市的药企君实生物(HK.01877)、信达生物(HK.01801)、恒瑞医药(SH.600276)以及进入II期和III期临床试验的康宁杰瑞、基石药业等企业的新药在肿瘤免疫治疗方面的突破,都将带来伴随诊断的需求和合作。 与此同时,刚刚登陆科创板的微芯生物(SH.688321)宣布和Pre-IPO阶段的基因企业诺禾致源合作,基于诺禾致源的伴随诊断基因检测方法,来预测西奥罗尼针对小细胞肺癌的II期临床试验的病人筛选分组以及药效。 国内基因和新药的联姻故事刚刚开始。 3. 产业协同:基因企业和药厂深入合作 而对外海外而言,基因和新药的联姻已渐入佳境。 2019年4月12日,强生旗下的厄达替尼erdafitinib (Balversa)作为针对FGFR改变的膀胱癌患者的第一种靶向药获得FDA批准。同日,FDA也批准了Qiagen旗下针对厄达替尼的伴随诊断试剂盒。 更多基因企业与药企的深入合作,参见表3: 表3:基因企业和药企的合作举例(来源/基因慧整理) FDA的医疗器械与设备中心公开表示,将继续鼓励基因诊断企业与药企合作“药物-伴随诊断”, 这对于严重的危及生命的、新型疾病的早期治疗和用药指导非常有意义。 4. 支付回路时间 FDA发布文件 要点 2014 Guidance for Industry: In Vitro Companion Diagnostic Devices 帮助新药研发早期确定伴随诊断的需求 2016 Principles for Codevelopment of an In Vitro Companion Diagnostic Device with a Therapeutic Product 帮助新药和伴随诊断IVD研发的实用指南 2018 Developing and Labeling In Vitro Companion Diagnostic Devices for a Specific Group or Class of Oncology Therapeutic Products 明确伴随诊断产品的分类,确定其治疗的意义 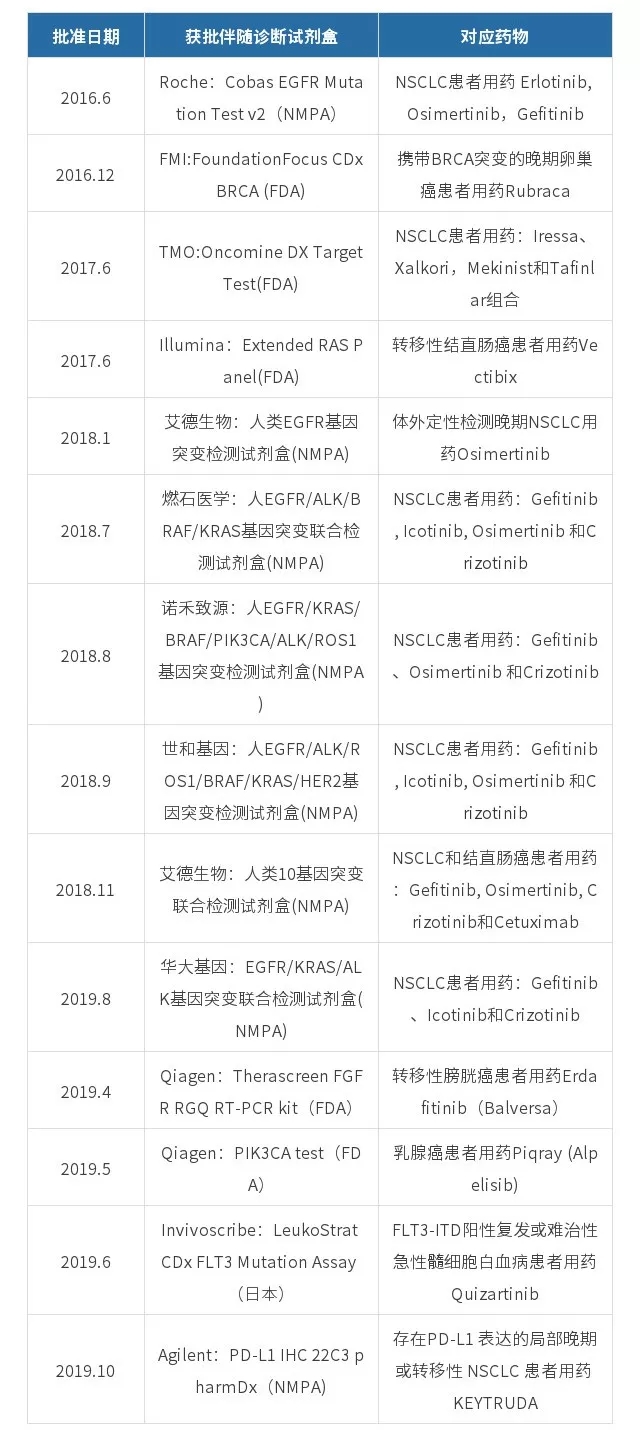
# 合作机构 合作开发 1 Cellgen & Genomics Testing Cooperative 免疫治疗伴随诊断 2 Qiagen & LabCorp 肺癌、乳腺癌、大肠癌、膀胱癌以及泛癌种的NGS/qPCR伴随诊断 3 Qiagen & Inovio Pharmaceuticals HPV宫颈发育不良的免疫治疗伴随诊断 4 Resolution Bioscience & Janssen 治疗前列腺癌药Niraparib的伴随诊断 5 Prometheus & Takeda 炎症性肠病(IBD)的伴随诊断 6 Thermo Fisher Scientific & Eli Lilly RET激酶抑制剂LOXO-292的伴随诊断