时间:2024-07-17 15:54

背景:
听力损失影响全球近4.66亿人,预计到2050年将影响超过9亿人。遗传因素在听力损失的发病机制中起着重要作用,高达55%的与年龄相关的听力损失归因于遗传。
对大家族的研究有助于鉴定与听力损失相关的一些基因,最近,全基因组和外显子组测序与家族病例相结合,促进了因果基因的识别。大量基因被鉴定为与非综合征性听力损失的单基因遗传相关(约130个),突出了该病的遗传复杂性,其中近50个与常染色体显性遗传性非综合征性听力损失(ADNSHL)相关。新基因仍有待鉴定,然而,鉴于支持听力损失起源的广泛遗传异质性,新鉴定的基因和变异很少在一个或几个系谱中发现,这使得通过可重复性确认它们成为一项具有挑战性的任务。因此,功能研究是验证遗传发现的关键。
结果:
一、临床表型汇总
一个5代巴西大家庭作为研究对象,受影响的个体表现为非综合征、进行性、感音神经性、双侧、中度至重度听力损失,听力损失的发病年龄从 4 岁到 35 岁不等,平均发病年龄为 12 岁。家系图见图1,具体临床表型见Table1。
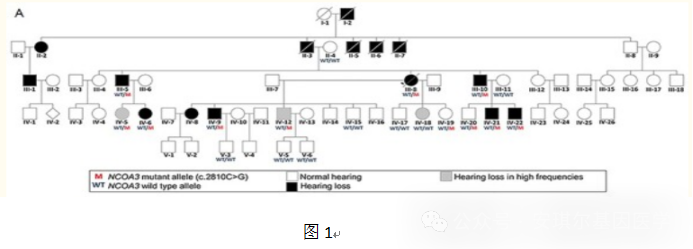
二、候选基因定位
作者首先通过50 K SNP 阵列分析将候选基因定位于20号染色体上。然后对两个受影响个体(III-8 和 III-10)的样本进行了全外显子组测序,通过Table2步骤进行过滤,发现可疑位点NCOA3基因NM_181659:c.2810C>G:p.Ser937Cys。通过对19 个样品进行sanger测序,发现该变异存在于所有 7 个受影响个体和 4 个未受影响个体的杂合子中。这4个未受影响的个体均在家庭中观察到的听力损失发病范围内(4-35岁),因此,听力损失的表现可能会在以后出现。
三、功能验证
对3个不同发育阶段(P4、P10 和 P16)的小鼠内耳组织切片进行了 RT-PCR 和免疫荧光,发现在所有时间点的耳蜗和带有血管纹的 Corti 器官中均检测到Ncoa3表达(图2A和2B)。斑马鱼整体原位杂交显示ncoa3在 3 和 5dpf 斑马鱼幼虫的耳囊中表达(图2C)。有趣的是,即使在耳系统完全发育后,仍有持续表达,如在幼鱼的内耳中检测到的(5 和 7wpf,受精后数周)(图 2C)。
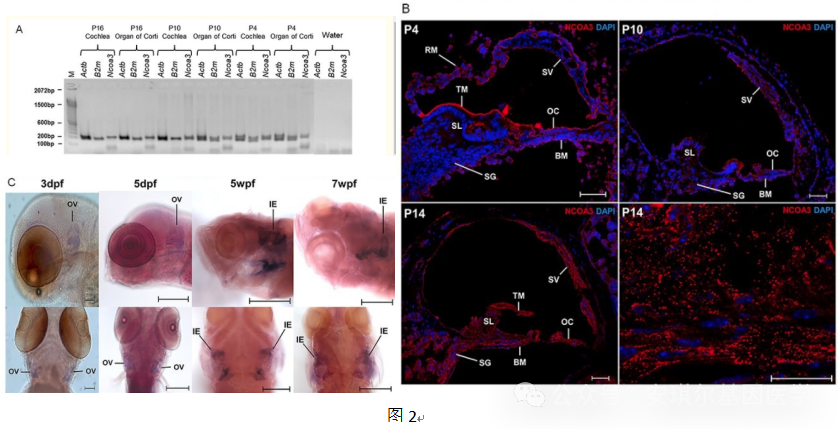
使用 CRISPR/Cas9 基因组编辑生成了ncoa3纯合斑马鱼突变体,ncoa3bi456/bi456(ncoa3−/−)携带 5 bp 缺失 (delTACGA),将ncoa3bi456/bi456杂交到携带Tg的双转基因系,斑马鱼ncoa3bi456/bi456在5dpf时没有显示任何主要的耳朵形态异常,但在 95% 的幼虫的嵴区域内检测到异常的软骨细胞簇(mcherry阳性)(图3A)。用phalloidin染色标记静纤毛的肌动蛋白丝,发现静纤毛杂乱无章的分布(图3B)。
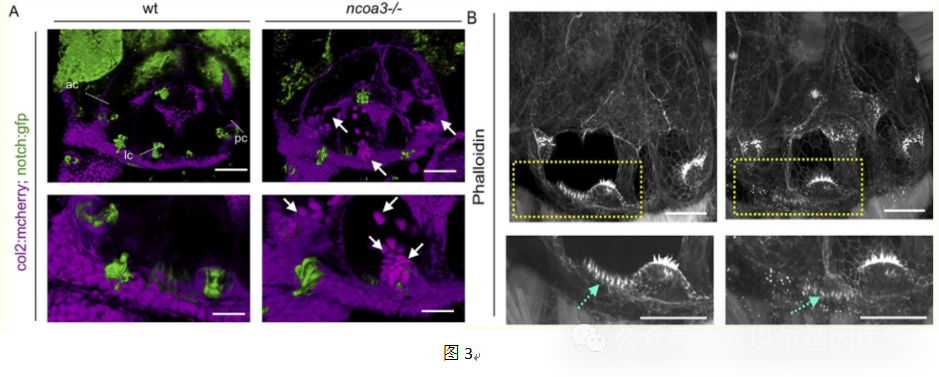
此外,作者还评估了ncoa3bi456/bi456成年斑马鱼耳的颅面骨密度和异位矿化,结果发现颅面骨的骨密度高,耳石在突变体中显示出骨矿物质密度增加,通过比较游泳轨迹发现ncoa3bi456/bi456突变体的空间分布异质性增加。
讨论:
通过将连锁分析与外显子组测序和功能分析相结合,首次报道了NCOA3 中罕见变异的分离与听力损失之间的关联,表明了导致听力障碍发病机制的新机制。NCOA3是来自NCOA基因家族的核受体共激活剂,正调节核受体介导的基因转录。作者在NCOA3 中发现了一个错义变体, c.2810C > G: p.Ser937Cys,其计算预测和频率与该变体导致听力损失的假设一致。在小鼠和斑马鱼耳朵中提供了进一步的表达数据,这表明耳朵中基因功能的进化保守。此外,通过 CRISPR/Cas9,生成了ncoa3斑马鱼基因敲除,以进一步研究ncoa3在发育和衰老过程中耳部功能丧失的影响。
尽管家庭规模不允许就 c.2810C > G 变异导致听力损失得出明确结论,但功能结果与NCOA3在听力中发挥作用的假设一致,表明骨骼稳态(软骨行为和骨密度)为病情的一个重要因素。作者的贡献是进一步引起人们对NCOA3 的关注,因为它可能与听力有关。